一种名为 AQAMAN 的合成小分子化合物可以预防甚至逆转与几种罕见的神经退行性疾病(包括聚谷氨酰胺(或 polyQ)疾病)相关的神经元中有害蛋白质的积累。
患有 polyQ 疾病(例如亨廷顿氏病和马查多-约瑟夫病)的人会失去肌肉控制和协调,因为大脑中的神经细胞会慢慢死亡。他们在平衡和步态以及说话和吞咽方面遇到越来越大的困难。这些遗传性疾病是由基因突变引起的,无法治愈;迫切需要药物治疗。
香港中文大学(CUHK)的生物化学家 Edwin Chan 在过去二十年一直研究 polyQ 疾病。他专注于神经元中的蛋白质如何以错误的方式折叠,以及这些错误折叠的蛋白质如何形成导致细胞死亡的有毒团块。
AQAMAN 代表针对 Machado-Joseph 相关神经变性的 Anti-polyQ 聚集,是由伊利诺伊大学香槟分校的合作者 Steven Zimmerman 及其同事合成的分子。它最初设计用于治疗肌肉萎缩症。在体外和果蝇中测试 AQAMAN 时,Chan 的团队,包括中大的同事 Jacky Ngo,发现该化合物抑制了神经元中毒性 polyQ 蛋白的积累。
“我们惊讶地发现 AQAMAN 会干扰神经细胞中有毒蛋白质的聚集,并希望它能带来新的疗法,从而缓解 polyQ 疾病患者的症状,”Chan 说。
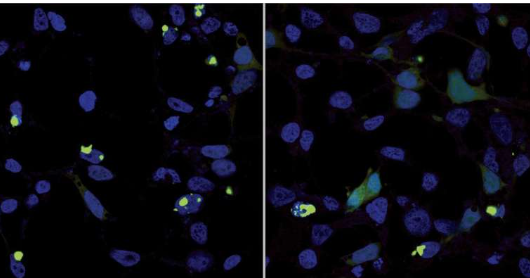
该团队曾预计 AQAMAN 会针对具有已知会产生有毒蛋白质的缺陷的 RNA 分子。然而,他们的分析发现,AQAMAN 实际上会导致蛋白质分散并作为细胞正常“自噬”过程的一部分被去除,在该过程中,细胞会消耗受损部分或废物。AQAMAN 分子与可溶形式的有毒蛋白质结合,但需要进一步研究以更详细地了解扩散机制。
该发现登上了《生物化学杂志》的封面,可以为开发治疗 polyQ 疾病的新药提供信息。该团队接下来计划在动物模型中测试 AQAMAN 的有效性。在考虑用于人类治疗之前,还需要制定药物输送策略。
